インフォメーション
【論文】鳴海教授の論文がOrg. Biomol. Chem.に掲載されました 2025/Apr
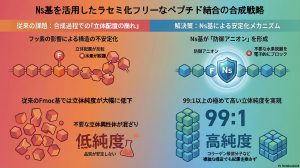
Ns基を用いたラセミ化フリーなペプチド結合形成戦略
· 論文タイトル:Racemization-free peptide bond formation via 2-nitrobenzensulfonyl strategy for diastereoselective synthesis of (Z)-fluoroalkene-type peptidomimetics (RSC出版)
· 年:2025(First published: 07 Apr 2025) (RSC出版)
· 掲載先:Organic & Biomolecular Chemistry(Issue 18, 2025 / 23, 4480–4486) (RSC出版)
· 著者:Chihiro Iio, Kohei Sato, Nobuyuki Mase, Tetsuo Narumi et al. (RSC出版)
· DOI:10.1039/D5OB00477B (RSC出版)
· URL:https://pubs.rsc.org/en/content/articlelanding/2025/ob/d5ob00477b (RSC出版)
研究の要点
フルオロアルケン型ペプチドイソスター(FADI)は、ペプチド結合の安定化に有用な骨格ですが、
フッ素の電子求引効果によりα位が酸性化し、活性化エステル形成時にジエノラートアニオンが生成、
ラセミ化が進行するという課題がありました。
本研究では、N末端保護基として2-ニトロベンゼンスルホニル(Ns)基を導入することで、塩基条件下でスルホンアミドアニオンを優先的に形成させ、α脱プロトン化を抑制することに成功しました。
その結果、99:1以上の高いジアステレオ選択性を実現し、コラーゲン模倣ペプチドやタウ由来R3ペプチドの合成においても、立体化学を保持したまま効率的な合成を達成しました。
※本稿は、掲載論文(URL)に基づき生成AIを用いて要約・表現を作成しています。内容の正確性には配慮していますが、解釈や表現の過程で不正確な記載が含まれる可能性があります。正式な情報は原論文をご確認ください。